相关试题
换一换


分子中,S原子成键的杂化轨道类型为()
A.杂化 B.sp杂化 C.杂化 D.不等性杂化
答案
在OF2分子中,氧原子成键的杂化轨道是下列中哪种杂化轨道()?
A.sp3杂化 B.sp杂化 C.sp2杂化 D.sp3不等性杂化
答案
SiF4分子中Si原子的成键杂化轨道应是()。
答案
同一原子内,s轨道和p轨道在成键时可以杂化
答案
下列分子中,其中心原子采取等性sp²杂化轨道成键的是()。
A.l₂Cl₆,分子中各原子不在同一平面 B.₂H₂,直线型分子 C.₂H₄,分子中各原子均在同一平面 D.NCl₃,原子不在同一平面
答案
下列分子中,中心原子不是采用sp^3d杂化轨道成键的是( )。
A.XeF2 B.ClF3 C.SF4 D.IF5
答案
NF3分子中N成键时所用杂化轨道类型是()
A.不等性sp3杂化 B.sp3 C.sp2 D.sp
答案
在下列物质的分子中,中心原子采用sp杂化轨道成键,分子空间构型是直线型的是( )。
A.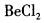 B.
B.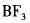 C.
C.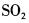 D.
D.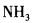
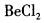 B.
B.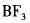 C.
C.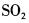 D.
D.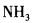
答案
中心原子仅以sp杂化轨道成键的是
答案
原子轨道发生杂化后可以增强成键能力
答案
热门试题
中国大学MOOC: HgCl2是直线形分子,Hg原子的成键杂化轨道是:
下列关于杂化轨道说法错误的是: 不是所有原子轨道都参与杂化 同一原子中能量相近的原子轨道参与杂化 杂化轨道中一定有一个电子 杂化轨道能量集中,有利于牢固成键
下列分子采取sp3杂化轨道成键的是:
中Be的原子轨道杂化轨道类型为()
下列说法中正确的是( )。: H2O分子中的O原子采用sp3杂化形成两个sp3杂化轨道,这两个sp3杂化轨道分别与H原子的1s轨道重叠形成两个化学键 中心原子采取sp杂化的分子构型是直线形 凡中心原子采用sp3杂化的分子,其分子空间构型必定是正四面体 同一原子中的任何轨道都可以参与杂化
凡是中心原子采用sp3d2杂化轨道成键的分子,其空间构型一定是八面体。
根据轨道杂化理论,BCl3分子的空间构型为 ,偶极矩 ,中心原子轨道杂化方式为 杂化;NF3分子的空间构型为 ,偶极矩 ,中心原子轨道杂化方式为 杂化
AB2型共价化合物,其中心原子均采用sp杂化轨道成键
BeCl2中Be的原子轨道杂化类型为:
BeC12中Be的原子轨道杂化类型为:
BeCl2中Be的原子轨道杂化类型为:
BeCl₂和OF₂同为AB₂型分子,它们的中心原子均采取sp杂化的方式成键。()
已知BCl3分子中,硼以sp2杂化轨道成键,则该分子的空间构型是()。
SnCl2分子和H2O分子的空间构型均为V型,表明它们的中心原子采取相同方式的杂化轨道成键
简述碳原子杂化轨道的类型及特点。
下列分子中,中心原子的轨道采取等性杂化的是( )
以sp2杂化轨道成键的BF3分子的空间构型是()
sp2杂化轨道的成键能力为()。
s轨道和p轨道杂化的类型有
杂化轨道理论认为,由于原子轨道侧面重叠所形成的共价键叫做σ键()



 使用微信扫一扫登录
使用微信扫一扫登录