用杂化轨道理论推测下列分子的空间构型.其中为正四面体的是( )。
A. SiH4
B. H3
C. lCHCl3
D. Br3
查看答案
相关试题
换一换


用杂化轨道理论推测下列分子的空间构型,其中为正四面体的是( )。
A.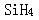 B.
B.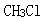 C.
C.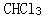 D.
D.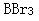
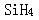 B.
B.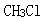 C.
C.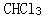 D.
D.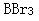
答案
用杂化轨道理论推测下列分子的空间构型.其中为正四面体的是( )。
A.SiH4 B.H3 C.lCHCl3 D.Br3
答案
用杂化轨道理论推测下列分子的空间构型.其中为正四面体的是()。
A.SiH4 B.CH3Cl C.CHCl3 D.BBr3
答案
用杂化轨道理论推测下列分子空间构型,其中为三角锥形的是( )。
A.NH3 B.H2O C.BF3 D.BeCl2
答案
用杂化轨道理论推测下列分子空间构型,其中为平面三角形的是( )。
A.NF3 B.AsH3 C.BF3 D.SbH3
答案
用杂化轨道理论推测下列分子的空间构型,其中为平面三角形的是()。
A.NF3 B.3 C.sH3 D.SbH3
答案
用杂化轨道理论推测下列分子的空间构型,其中为平面三角形的是:
A.NF3 B.BF3 C.AsH3 D.SbH3
答案
用杂化轨道理论推测下列分子的空间构型,其中为平面三角形的是:
A.NF3 B.AsH3 C.BF3 D.SbH3
答案
用杂化轨道理论推测下列分子的空间构型,其中为平面三角形的是:
A.NF3 B.BF3 C.ASH3 D.SbH3
答案
当分子的中心原子以s p 3 杂化成键时,分子的空间构型为四面体
答案
热门试题
下列分子空间构型是四面体形的是(??? )
甲烷,化学式CH4,分子是正四面体空间构型()
“下列各种粒子,分子构型是正四面体的是( )。
下列配离子空间构型为正四面体的是
试用杂化轨道理论说明MgCl2分子的空间构型
下列说法中正确的是( )。: H2O分子中的O原子采用sp3杂化形成两个sp3杂化轨道,这两个sp3杂化轨道分别与H原子的1s轨道重叠形成两个化学键 中心原子采取sp杂化的分子构型是直线形 凡中心原子采用sp3杂化的分子,其分子空间构型必定是正四面体 同一原子中的任何轨道都可以参与杂化
下列物种几何构型为正四面体的是()
下列分子和离子中,中心原子的价层电子对几何构型为四面体,且分子(离子)空间构型为角形(V形)的是
根据VSEPR理论,SF4的空间构型为??? ???????????????????????????( ??) A. T形??? B. V形???? C.? 变形四面体?? D. 三角锥??? E. 正四面体
用杂化理论推测,分子的空间构型为平面三角形的是()。
用杂化理论推测,分子的空间构型为平面三角形的是()。
中国大学MOOC: 凡是以sp3形式杂化的分子,必定是四面体结构
根据轨道杂化理论,BCl3分子的空间构型为 ,偶极矩 ,中心原子轨道杂化方式为 杂化;NF3分子的空间构型为 ,偶极矩 ,中心原子轨道杂化方式为 杂化
形成CCl4时,C原子采取了sp3轨道杂化,所以其结构是正四面体
分子的空间构型总是和中心原子的杂化轨道空间构型相同。
下列可证明甲烷分子是正四面体结构的是()
试用轨道杂化理论说明:CH4是正四面体,NH3是三角锥形,而H2O是V(角)形
试用轨道杂化理论说明:CH4是正四面体,NH3是三角锥形,而H2O是V(角)形
任何中心离子配位数为4的配离子,均为四面体构型
燃烧四面体为()



 使用微信扫一扫登录
使用微信扫一扫登录