高中化学学科知识与教学能力试题(二)
考试总分:150分
考试类型:模拟试题
作答时间:120分钟
已答人数:422
试卷答案:有
试卷介绍: 高中化学学科知识与教学能力考什么?高中化学学科知识与教学能力试题(二)为您解答。
试卷预览
-
1. 发现法的广泛使用被限制的原因是()。①学生不愿发现②需要大量财力、物力③教师消耗大量精力④学生困难大⑤学习费时太多⑥一切知识都不需要发现
A①②⑤⑥
B②③④⑤
C③④⑤⑥
D①③④⑤
-
2. 下列有关物质结构的说法中正确的是( )。
A石油裂解只破坏极性键
B含极性键的共价化合物一定是电解质
C氯化钠固体中的离子键在溶于水时被破坏
DHF的分子间作用力大于HCl,故HF比HCl稳定
-
3. 用括号内试剂及操作方法除去下列各物质中的少量杂质,不正确的是( )。
A苯中的苯酚(溴水、过滤)
B乙酸乙酯中的乙酸(饱和碳酸钠溶液、分液)
C溴乙烷中的乙醇(水、分液)
D溴苯中的溴(NaOH溶液、分液)
-
4. 实验者是化学实验的主体,其根本属性是()。
A主体性
B社会性
C物质性
D特殊性
-
5. 具有安全意识和严谨的科学态度,具有探索未知、崇尚真理的意识反应的化学学科核心素养是( )。
A宏观辨识与微观探析
B证据推理和模型认知
C科学探究与创新意识
D科学精神与社会责任
-
6. 在《普通高中化学课程标准(实验)》中,“知道化学键的断裂和形成是化学反应中能量变化的主要原因”内容标准对应的课程模块是( )。
A化学2
B化学与技术
C物质结构与性质
D化学反应原理
-
7. 下列关于高中课程结构的叙述不正确的是( )。
A高中化学课程由若干课程模块构成,分为必修、选修两类
B必修包括2个模块,选修包括5个模块
C每个课程模块2学分,36学时
D有机化学基础属于选修模块
-
8. 下列选项内容不属于试题的质量指标的是( )。
A标准度
B信度
C难度
D效度
-
9. 建立在真实、有感染力的化学事件或问题基础上的教学是( )。
A支架式教学
B情境式教学
C探究式教学
D启发式教学
-
10. 以下有关个体内差异评价的说法错误的是( )。
A个体内差异评价有利于减轻学生的心理负担和压力,增强自信心,强化学习动力
B这种评价的结果往往难以反映个体问的差异,也无法确定被评价者达成教育目标的程度
C一个学生化学成绩持续提高,教师就可以做出该生已有进步的评价
D被评价者自己参照评价指标体系对自己的活动状况或发展状况进行自我鉴定
-
11. 香豆素是一种天然香料,存在于黑香豆、兰花等植物中,结构如图2所示,下列说法不正确的是( )。

A香豆素的分子式为C9H6O2
B在一定条件下,香豆素能与H2发生加成反应
C香豆素可使酸性KMnO4溶液褪色
D香豆素属于芳香烃
-
12.
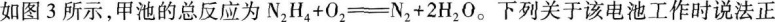 确的是( )。
确的是( )。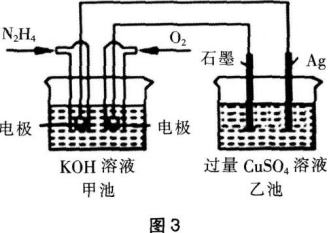
A
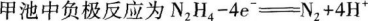
B甲池溶液pH不变,乙池溶液pH减小
C反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度
D甲池中消耗2.24LO2,此时乙池中理论上最多产生12.8g固体
-
13. 化学新课程实施中.最有利于促进学生学习方式改变、提高学生科学素养的一种评价方法是( )。
A纸笔诊断性测验评价
B纸笔总结性测验评价
C档案袋评价
D活动表现评价
-
14. 作为课堂教学的“科学探究”,其主要环节有( )。
A选题、论证、假设、计划、实施
B提出问题、猜想与假设、制订计划、进行实验、收集证据、解释与结论、反思与评价、表达与交流
C观察、实验、测定、数据处理、科学抽象、理想模型、假说、验证、得出结论
D调查、分析、假设、设计方案、实施、收集并处理数据、验证方案、得出结论
-
15. 在普通高中化学课程标准中“了解居室装修材料的主要成分及其作用”内容标准对应的课程模块是( )。
A化学1
B化学与生活
C物质结构与性质
D实验化学
-
16.
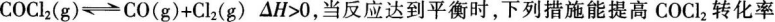 的是( )。
的是( )。
①升温
②恒容通入惰性气体
③增加CO浓度
④减压
⑤催化剂
⑥恒压通入惰性气体A①②④
B①④⑥
C②③⑥
D③⑤⑥
-
17. 化学键使得100多种元素组成了世界的万物。下列关于化学键的叙述正确的是( )。
A离子化合物中一定含共价键,共价化合物中不含离子键
B共价化合物中可能含离子键,离子化合物中只含离子键
C构成单质分子的粒子一定含有共价键
D在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用
-
18. 有关下列电化学装置的说法中正确的是( )。
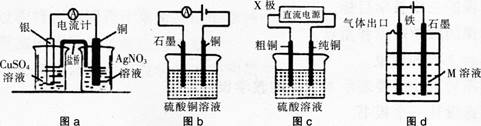
A图a是原电池装置。可以实现化学能转化为电能
B图b电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度
C图C中的X极若为负极,则该装置可实现粗铜的精炼
D图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
-
19. 下列说法正确的是( )。
A在101kPa时,1molC和适量的O2反应,生成1molCO时,放出110.5kJ热量,则C的燃烧热为110.5kJ/mol
B在101kPa时,1mol的H2完全燃烧生成水蒸气,放出285.8kJ热量,则H2的燃烧热为-285.8kJ/mol
C
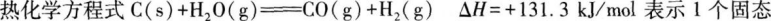 C原子和1分子水蒸气反应吸热131.3kJ
C原子和1分子水蒸气反应吸热131.3kJ
D
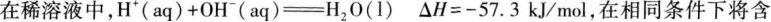 0.5molH2SO4的浓硫酸与1molBa(OH)2的水溶液混合,放出的热量大于57.3kJ
0.5molH2SO4的浓硫酸与1molBa(OH)2的水溶液混合,放出的热量大于57.3kJ
-
20. 在含有下列离子组的溶液中,加入Fe(N03)2固体后,仍然能够大量共存的离子组是( )。
AK+、SO42-、NH4+、CO32-
BK+、Ba2+、SO42-、Cl-
CNa+、H+、Cl-、SO42-
DNa+、Mg2+、Cl-、NO3-
-
1. 阅读下面文字,回答有关问题。
化学学科主题是具有共同学科属性的一类化学知识的整体,因而具有相对完整性,能够形成一个从基本概念到核心概念再到学科大概念的相对完整的体系结构。基于化学学科核心素养发展的课堂教学设计需要树立“整体观”,应围绕化学学科主题来确定其素养发展的价值,而不应只局限于“局部”(如课时教学内容)进行“标签式”的所谓“素养为本”的教学设计。
问题:
(1)以“典型金属及其化合物的性质”主题为例说明这一主题素养发展设计。
(2)“典型金属及其化合物的性质”这一主题的素养发展价值有哪些?
-
2. 化学教学过程是以化学知识为载体的多向互动过程,体现了教学过程中活动与过程的多维性。
(1)请用相关化学教学理论简单分析图2的含义。
(2)请简述新课程改革背景下化学评价观的相关内容。
-
1. 某化学教师在一次化学测验中设计了下面试题,并对学生的解题结果进行了统计和分析。
试题:金属(M)-空气电池(如图3)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为: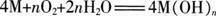
已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )。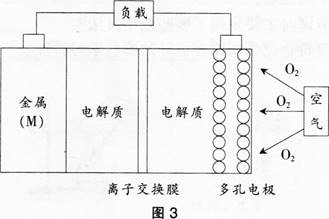 A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.在M9-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
C.M-空气电池放电过程的正极反应式为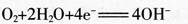
D.比较M9、Al、Zn三种金属一空气电池,M9-空气电池的理论比能量最高
【考试结果】选A的几乎没有,选B的有21%,选c的有43%,选D的有36%。试根据上述信息,回答下列问题:
(1)本题的正确选项是什么?
(2)请分析和诊断各个选项解答错误的原因。
(3)如果要你讲评本题,你教给学生的正确思路是什么?
-
1. 以下材料为某教师对“乙烯的结构”知识的教学过程片段:
【回顾旧知】引导学生画出乙烷的电子式和结构式。
【提出问题】若将乙烷在隔绝空气条件下受强热发生分解,得到等物质的量的两种气体,试写出这两种气体物质的化学式,并给予必要的提示:其中一种气体是氢气。
【学生活动】学生不难写出另一种气体的化学式是C2H4。
【提出问题】C2H4是什么?它的结构是什么样的?
【师生互动】首先,从分子组成上看,该气体分子(C2H4)与乙烷具有相同的碳原子,但少两个氢原子。随即展示乙烷的球棍模型,拿掉两个“氢原子”,问:剩余的两个键怎么办?追问:那么原来的碳氢键的角度会变化吗?接着.辅以Flash动画演示乙烷的立体模型转变为乙烯的平面模型的过程,让学生直观地看出乙烯的结构特征。反问:C2H4分子与乙烷分子的几何构型一样吗?
两个碳原子间共用的电子对数目相同吗?碳碳键间键长、牢固程度相同吗?
【学生活动】学生分组,自主讨论。
根据以上材料,回答下列问题:
(1)该教师在教授本节课时主要采用了哪些教学方法?
(2)材料中的教学过程符合化学新课程倡导的哪些学习特征?
-
1. 阅读下列材料,按要求完成教学设计任务。
材料一《普通高中化学课程标准(实验)》内容标准为:“通过实验了解氯、氮、硫、硅等非金属及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响”。活动与探究建议:“实验氯气的漂白性”。
材料二某高中化学教科书《化学1》“氯气与水的反应”的教学片段。
目前,很多自来水厂用氯气来杀菌、消毒,我们偶尔闻到的自来水散发出的刺激性气味就是余氯的气味。
氯气溶于水为什么能杀菌消毒呢?在25℃时,1体积的水可溶解约2体积的氯气.氯气的水溶液称为氨水。在常温下,溶于水中的部分Cl2与水发生如下反应: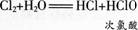
次氯酸(HClO)具有强氧化性,因此,次氯酸能杀死水中的病菌,起到消毒的作用。氯水也因为含有次氯酸而具有漂白作用。
次氯酸是很弱的酸,不稳定,只存在于水溶液中,在光照下易分解放出氧气:
近年来有科学家提出,使用氯气对自来水消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此,人们已开始研究并试用新的自来水消毒剂。如二氧化氯(CLO2)、臭氧等。

最初,人们直接用氯气作漂白剂,但因氯气的溶解度不大,而且生成的HClO不稳定,难以保存,使用起来很不方便,效果也不理想,在CL2与水反应原理的基础上,经过多年的实验、改进,才有了今天常用的漂白液和漂白粉。
材料三教学对象为高中一年级学生,他们已经学过了实验的基本方法,物质的量,氧化还原反应,金属及其化合物的相关知识。
要求:
结合上述材料,完成“氯气与水的反应”片段的教学设计,包括教学目标,教学重、难点,教学过程,板书设计(不少于300字)。